2.4. Структура веществ с ненаправленным взаимодействием
В настоящее время в результате систематических структурных исследований накоплен достаточно обширный материал по определению структуры самых различных веществ. Эти данные позволяют установить ряд соотношений между химическим составом твердого тела, характером сил межатомного взаимодействия в нем, пространственным расположением этих атомов и физическими свойствами. Закономерности в строении кристаллов, установленные с помощью структурного анализа, часто оказываются настолько общими, что могут сами быть использованы при анализе еще не исследованных веществ. Это во многих случаях позволяет построить модели структуры, что облегчает и упрощает задачу структурного исследования, поскольку сводит ее к проверке правильности той или иной модели [51, 54, 55].
Выше (гл. 1, раздел 1.5) нами был рассмотрен принцип плотной упаковки. Этот принцип играет очень важную роль в определении типа кристаллических структур различных классов веществ. Он лежит в основе установления конфигурации частиц в тех случаях, когда между частицами действуют ненасыщенные и ненаправленные связи. В этих условиях энергетически более выгодным оказывается образование структуры с возможно большими координационными числами n. Рассмотрим такие типы структур.
Металлы
Как уже было сказано выше, в
кристаллах с металлической связью обобществляются валентные электроны в
пределах всего кристалла. При этом наиболее вероятным становится образование
структур типа плотных шаровых упаковок. Результаты структурного анализа
показывают, что металлы кристаллизуются, за немногими исключениями, в трех
структурных типах: кубической и гексагональной плотной упаковке (рис. 1.16,
1.17), а также в кубической объемноцентрированной решетке (рис. 1.7, а). При
этом в двух первых случаях координационное число ![]() , а коэффициент
упаковки h,
показывающий, какая доля объема элементарной ячейки занята атомами, составляет
значение 74,04 %. Для ОЦК структуры
, а коэффициент
упаковки h,
показывающий, какая доля объема элементарной ячейки занята атомами, составляет
значение 74,04 %. Для ОЦК структуры ![]() , а h =
68,1%. Объемноцентрированный куб по
коэффициенту упаковки незначительно отличается от простого куба, имеющего атомы
только в вершинах (
, а h =
68,1%. Объемноцентрированный куб по
коэффициенту упаковки незначительно отличается от простого куба, имеющего атомы
только в вершинах (![]() ,
, ![]() ), однако в «рыхлой»
структуре простого куба не кристаллизуется ни один металл.
), однако в «рыхлой»
структуре простого куба не кристаллизуется ни один металл.
Ионные кристаллы
Ионы с заполненными
валентными оболочками обладают сферической симметрией. Кулоновские силы между
ионами (ионная связь) с большой степенью приближения можно считать центральными
силами. Однако отличие случая ионной связи от задачи о плотных шаровых
упаковках заключается в том, что ионы имеют различные ионные радиусы (![]() − радиус катиона,
− радиус катиона, ![]() − радиус аниона)
и электрические заряды разного знака. Образование катионов и анионов из
нейтральных атомов происходит соответственно путем отдачи и присоединения
внешних электронов. Поэтому, как правило, радиусы анионов больше радиусов
катионов. Понятие о радиусе иона
является, конечно, не чисто геометрическим и характеризует радиус «сферы действия» данного иона. Анионы −
основные по объему «кирпичи» в структуре ионного кристалла. Это хорошо видно из
анализа данных, приведенных в табл. 2.6 [98].
− радиус аниона)
и электрические заряды разного знака. Образование катионов и анионов из
нейтральных атомов происходит соответственно путем отдачи и присоединения
внешних электронов. Поэтому, как правило, радиусы анионов больше радиусов
катионов. Понятие о радиусе иона
является, конечно, не чисто геометрическим и характеризует радиус «сферы действия» данного иона. Анионы −
основные по объему «кирпичи» в структуре ионного кристалла. Это хорошо видно из
анализа данных, приведенных в табл. 2.6 [98].
Таблица 2.6
Атомные и ионные радиусы элементов
|
Номер |
Символ |
Атомный |
Ион |
Ионный |
Номер |
Символ |
Атомный |
Ион |
Ионный |
|
1 |
H |
0,046 |
H- |
0,154 |
45 |
Rh |
0,134 |
Rh3+ |
0,068 |
|
2 |
He |
– |
– |
– |
|
|
|
Rh4+ |
0,065 |
|
3 |
Li |
0,152 |
Li+ |
0,078 |
46 |
Pd |
0,137 |
Pd2+ |
0,050 |
|
4 |
Be |
0,114 |
Be2+ |
0,054 |
47 |
Ag |
0,144 |
Ag+ |
0,113 |
|
5 |
B |
0,097 |
B3+ |
0,02 |
48 |
Cd |
0,150 |
Cd2+ |
0,103 |
|
6 |
C |
0,077 |
C4+ |
<0,02 |
49 |
In |
0,157 |
In3+ |
0,092 |
|
7 |
N |
0,071 |
N5+ |
0,01-0,02 |
50 |
Sn |
0,158 |
Sn4- |
0,215 |
|
8 |
O |
0,060 |
O2- |
0,132 |
|
|
|
Sn4+ |
0,074 |
|
9 |
F |
– |
F– |
0,133 |
51 |
Sb |
0,161 |
Sb3+ |
0,090 |
|
10 |
Ne |
0,160 |
– |
– |
52 |
Te |
0,143 |
Te2- |
0,211 |
|
11 |
Na |
0,186 |
Na+ |
0,098 |
|
|
|
Te4+ |
0,089 |
|
12 |
Mg |
0,160 |
Mg2+ |
0,078 |
53 |
I |
0,136 |
I- |
0,220 |
|
13 |
Al |
0,143 |
Al3+ |
0,057 |
|
|
|
I5+ |
0,094 |
|
14 |
Si |
0,117 |
Si4– |
0,198 |
54 |
Xe |
0,218 |
– |
– |
|
|
|
|
Si4+ |
0,039 |
55 |
Cs |
0,265 |
Cs+ |
0,165 |
|
15 |
P |
0,109 |
P5+ |
0,03-0,04 |
56 |
Ba |
0,217 |
Ba2+ |
0,143 |
|
16 |
S |
0,106 |
S2– |
0,174 |
57 |
La |
0,187 |
La3+ |
0,122 |
|
|
|
|
S6+ |
0,034 |
58 |
Ce |
0,182 |
Ce3+ |
0,118 |
|
17 |
Cl |
0,107 |
Cl– |
0,181 |
|
|
|
Ce4+ |
0,102 |
|
18 |
Ar |
0,192 |
– |
– |
59 |
Pr |
|
Pr3+ |
0,116 |
|
19 |
K |
0,231 |
K+ |
0,133 |
|
|
|
Pr4+ |
0,100 |
|
20 |
Ca |
0,197 |
Ca2+ |
0,106 |
60 |
Nd |
|
Nd3+ |
0,115 |
|
21 |
Sc |
0,160 |
Sc2+ |
0,083 |
61 |
Pm |
|
Pm3+ |
0,106 |
|
22 |
Ti |
0,147 |
Ti2+ |
0,076 |
62 |
Sm |
|
Sm3+ |
0,113 |
|
|
|
|
Ti3+ |
0,069 |
63 |
Eu |
|
Eu3+ |
0,113 |
|
|
|
|
Ti4+ |
0,064 |
64 |
Gd |
|
Gd3+ |
0,111 |
|
23 |
V |
0,132 |
V3+ |
0,065 |
65 |
Tb |
|
Tb3+ |
0,109 |
|
|
|
|
V4+ |
0,061 |
|
|
|
Tb4+ |
0,089 |
|
|
|
|
V5+ |
~0,04 |
66 |
Dy |
|
Dy3+ |
0,107 |
|
24 |
Cr |
0,125 |
Cr3+ |
0,064 |
67 |
Ho |
|
Ho3+ |
0,105 |
|
|
|
|
Cr6+ |
0,03-0,04 |
68 |
Er |
|
Er3+ |
0,104 |
|
25 |
Mn |
0,112 |
Mn2+ |
0,091 |
69 |
Tm |
|
Tm3+ |
0,104 |
|
|
|
|
Mn3+ |
0,070 |
70 |
Yb |
|
Yb3+ |
0,100 |
|
|
|
|
Mn4+ |
0,052 |
71 |
Lu |
|
Lu3+ |
0,099 |
|
26 |
Fe |
0,124 |
Fe2+ |
0,087 |
72 |
Hf |
|
Hf4+ |
0,084 |
|
|
|
|
Fe3+ |
0,067 |
73 |
Ta |
|
Ta5+ |
0,068 |
|
27 |
Co |
0,125 |
Co2+ |
0,082 |
74 |
W |
|
W4+ |
0,068 |
|
|
|
|
Co3+ |
0,065 |
|
|
|
W6+ |
0,065 |
|
28 |
Ni |
0,125 |
Ni2+ |
0,078 |
75 |
Re |
|
Re4+ |
0,072 |
|
29 |
Cu |
0,128 |
Cu+ |
0,096 |
76 |
Os |
|
Os4+ |
0,067 |
|
|
|
|
Cu2+ |
0,072 |
77 |
Ir |
|
Ir4+ |
0,066 |
|
30 |
Zn |
0,133 |
Zn2+ |
0,083 |
78 |
Pt |
|
Pt2+ |
0,052 |
|
31 |
Ga |
0,135 |
Ga3+ |
0,062 |
|
|
|
Pt4+ |
0,055 |
|
32 |
Ge |
0,122 |
Ge4+ |
0,044 |
79 |
Au |
|
Au+ |
0,137 |
|
33 |
As |
0,125 |
As3+ |
0,069 |
80 |
Hg |
|
Hg2+ |
0,112 |
|
|
|
|
As5+ |
~0,04 |
81 |
Tl |
|
Tl+ |
0,149 |
|
34 |
Se |
0,116 |
Se2– |
0,191 |
|
|
|
Tl3+ |
0,106 |
|
|
|
|
Se6+ |
0,03-0,04 |
82 |
Pb |
|
Pb4- |
0,215 |
|
35 |
Br |
0,119 |
Br– |
0,196 |
|
|
|
Pb2+ |
0,132 |
|
36 |
Kr |
0,197 |
– |
– |
|
|
|
Pb4+ |
0,084 |
|
37 |
Rb |
0,251 |
Rb+ |
0,149 |
83 |
Bi |
|
Bi3+ |
0,120 |
|
38 |
Sr |
0,215 |
Sr2+ |
0,127 |
84 |
|
|
Po6+ |
0,067 |
|
39 |
Y |
0,181 |
Y3+ |
0,106 |
85 |
At |
|
At7+ |
0,062 |
|
40 |
Zr |
0,158 |
Zr4+ |
0,087 |
86 |
Rn |
|
– |
|
|
41 |
Nb |
0,143 |
Nb4+ |
0,074 |
87 |
Fr |
|
Fr+ |
0,180 |
|
|
|
|
Nb5+ |
0,069 |
88 |
Ra |
|
Ra+ |
0,152 |
|
42 |
Mo |
0,136 |
Mo4+ |
0,068 |
89 |
Ac |
|
Ac3+ |
0,118 |
|
|
|
|
Mo6+ |
0,065 |
90 |
Th |
|
Th4+ |
0,110 |
|
43 |
Tc |
– |
– |
– |
91 |
Pa |
|
– |
|
|
44 |
Ru |
0,134 |
Ru4+ |
0,065 |
92 |
U |
|
U4+ |
0,105 |
Эффективные электрические
поля (![]() ) при одинаковости зарядов
у катионов больше, чем у анионов, поэтому потенциальная энергия связи в
ионном кристалле в основном определяется энергией кулоновского взаимодействия
ионов. Минимум кулоновской энергии требует осуществления конфигурации с
чередованием ионов разного знака, что проявляется в шахматном законе
чередования ионов в кристалле хлористого натрия (рис. 1.19).
) при одинаковости зарядов
у катионов больше, чем у анионов, поэтому потенциальная энергия связи в
ионном кристалле в основном определяется энергией кулоновского взаимодействия
ионов. Минимум кулоновской энергии требует осуществления конфигурации с
чередованием ионов разного знака, что проявляется в шахматном законе
чередования ионов в кристалле хлористого натрия (рис. 1.19).
Рассмотрим ионный кристалл
простейшего состава AB. Координационные числа для
катионов и анионов при таком составе одинаковы (![]() ). Каждый катион стремится окружить себя возможно большим
числом анионов. Из-за взаимного отталкивания анионов при определенном их числе
возникнут симметричные конфигурации анионов с максимальным их удалением друг от
друга. Число анионов, которым может окружить себя данный катион, зависит от
отношения ионных радиусов
). Каждый катион стремится окружить себя возможно большим
числом анионов. Из-за взаимного отталкивания анионов при определенном их числе
возникнут симметричные конфигурации анионов с максимальным их удалением друг от
друга. Число анионов, которым может окружить себя данный катион, зависит от
отношения ионных радиусов ![]() . Чем меньше это отношение, тем меньше координационное число
иона. Предельные отношения ионных радиусов определяют границы устойчивости
соответствующих конфигураций и тем самым последовательность смены структурных
типов. Конфигурации с нечетными координационными числами
. Чем меньше это отношение, тем меньше координационное число
иона. Предельные отношения ионных радиусов определяют границы устойчивости
соответствующих конфигураций и тем самым последовательность смены структурных
типов. Конфигурации с нечетными координационными числами ![]() не удовлетворяют
требованию симметрии и эквивалентности анионов. Значения минимальных, или
критических, отношений
не удовлетворяют
требованию симметрии и эквивалентности анионов. Значения минимальных, или
критических, отношений ![]() , соответствующих
допустимым координационным числам, приведены в табл. 2.7.
, соответствующих
допустимым координационным числам, приведены в табл. 2.7.
Таблица 2.7
Критические
отношения радиусов ионов для различных координационных чисел
|
Координационные числа ионов |
Конфигурация ионов |
Критическая величина |
|
2 |
Друг против друга |
0,000 |
|
3 |
В вершинах равностороннего треугольника |
|
|
4 |
В вершинах тетраэдра |
|
|
4 |
В вершинах квадрата |
|
|
6 |
В вершинах октаэдра |
|
|
8 |
В вершинах куба |
|
|
12 |
Расположение плотной упаковки |
1,0 |
Эти значения вычислены из условия контакта катиона с окружающими его анионами и впервые были указаны Магнусом.
Опыт показывает, что для
кристаллов, состоящих из слабо поляризуемых ионов, координационные числа
действительно определяются соотношением ионных радиусов. Так, соединения типа
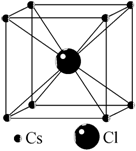
АВ (CsCl, CsBr, CsI) все имеют структуру типа CsCl (рис. 2.13) с
координационным числом n = 8, причем для всех этих веществ
отношение радиусов ионов лежит выше 0,73. Щелочно-галоидные соли, например NaCl, KCl, NaBr, имеющие отношение ионных радиусов меньше, чем 0,73, но
больше, чем 0,414, кристаллизуются в решетках типа NaCl (рис. 1.19)
с координационным числом ![]() . Структуры, относящиеся к типу a-ZnS (сфалерита) (рис. 1.21),
имеют координационное число
. Структуры, относящиеся к типу a-ZnS (сфалерита) (рис. 1.21),
имеют координационное число ![]() .
.
|
|
|
Рис. 2.13. Структура ионного кристалла CsCl |
Для ![]() нельзя образовать
трехмерную структуру, удовлетворяющую требованию чередования разноименных ионов.
Степень ионности структуры уменьшается с уменьшением координационного
числа n, и
соответственно возрастает доля ковалентной связи. Если в данном соединении
отношение ионных радиусов близко к критическому, то возможно полиморфное превращение, заключающееся в
переходе от одного структурного типа к другому. Например, в галогенидах рубидия
(RbCl, RbBr, RbI) такое превращение под действием
высокого давления заключается в переходе от структуры типа CsCl к типу NaCl.
нельзя образовать
трехмерную структуру, удовлетворяющую требованию чередования разноименных ионов.
Степень ионности структуры уменьшается с уменьшением координационного
числа n, и
соответственно возрастает доля ковалентной связи. Если в данном соединении
отношение ионных радиусов близко к критическому, то возможно полиморфное превращение, заключающееся в
переходе от одного структурного типа к другому. Например, в галогенидах рубидия
(RbCl, RbBr, RbI) такое превращение под действием
высокого давления заключается в переходе от структуры типа CsCl к типу NaCl.
Для
структур металлов и ионных кристаллов характерны значения координационных чисел
![]() , правильное и высокосимметричное расположение частиц в
пространстве с образованием трехмерного мотива. Такие структуры называются координационными.
, правильное и высокосимметричное расположение частиц в
пространстве с образованием трехмерного мотива. Такие структуры называются координационными.
Молекулярные кристаллы
Молекулы представляют группы атомов, соединенных прочными химическими связями, насыщенными в пределах каждой молекулы. Между молекулами действуют только слабые силы притяжения Ван-дер-Ваальса. Под действием этих ненаправленных и ненасыщенных сил образуются плотные упаковки молекул. В свою очередь, молекулы могут иметь различную форму: плоские и трехмерные группы атомов, кольца, цепочки и т. д. В отличие от ионных кристаллов, где силы связи между ионами являются центральными, для молекулярных кристаллов они не являются таковыми. Поэтому условия плотной упаковки молекул более сложны и приводят к тому, что молекулярные кристаллы обладают низкой симметрией, в отличие от высокой симметрии координационных кристаллов. Исключением из этого являются молекулярные кристаллы, образованные химически инертными элементами (He, Ne, Ar, Kr, X), атомы которых сферически симметричны и имеют заполненные электронные оболочки. Из-за слабого вандерваальсового взаимодействия при обычных температурах эти элементы находятся в газообразном состоянии. При достаточно низких температурах они образуют кристаллы со структурой гранецентрированного куба (рис. 1.7, e).
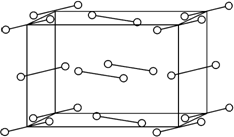
Следующими в порядке роста сложности являются двухатомные симметричные молекулы А2, имеющие гантелеобразную форму. Такие молекулы образуют атомы галогенов, и эти молекулы существуют как в газообразной, так и в жидкой и кристаллической фазах. На рис. 2.14 приведена элементарная ячейка, характерная для кристаллов галогенов J2, Cl2, Br2, и др. [83].
|
|
|
Рис. 2.14. Структурный тип йода (такую же структуру имеют кристаллы
хлора и брома) |
Рассмотрим
структуру молекулярного хлора. Кристалл молекулярного хлора имеет ромбическую
ячейку, в вершинах и центрах граней которой расположены двухатомные молекулы Cl2. Расстояние
между атомами в молекуле Cl2
составляет 2,02 Å. Расстояние до атомов Cl ближайших соседних молекул 3,34
Å. Первое расстояние соответствует прочной ковалентной связи между
атомами хлора, а второе − слабым вандерваальсовым связям между
молекулами. Молекулярное координационное число в кристалле хлора ![]() . На рис. 2.14 видно, что молекулы Cl2 в разных узлах решетки
расположены под некоторым углом друг к другу. Такое расположение вполне
закономерно и следует из принципа плотной упаковки, который запрещает
существование в молекулярных структурах плоскостей симметрии, перпендикулярных
координатным осям.
. На рис. 2.14 видно, что молекулы Cl2 в разных узлах решетки
расположены под некоторым углом друг к другу. Такое расположение вполне
закономерно и следует из принципа плотной упаковки, который запрещает
существование в молекулярных структурах плоскостей симметрии, перпендикулярных
координатным осям.
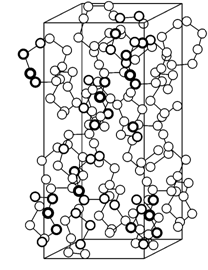
Более
сложным образом кристаллизуются селен и сера. Молекула ромбической модификации
серы построена из восьми атомов. В элементарной ячейке содержится 16 таких
молекул, а сама ячейка представляет собой четыре гранецентрированные ячейки,
вставленные одна в другую (рис. 2.15).
|
|
|
Рис. 2.15. Структура ромбической модификации серы [83] |
При упаковке несимметричных молекул образуется периодическая структура низкосимметричного кристалла с косоугольной элементарной ячейкой. Пустоты между молекулами, в отличие от симметричных пустот шаровых упаковок, в данном случае имеют неправильную форму.