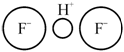2.3.5. Водородная связь
Поскольку нейтральный атом водорода имеет только один электрон, он должен обладать одной связью, позволяющей ему вступать в соединение лишь с каким-либо одним атомом другого сорта. Однако зачастую ядро атома водорода H+ оказывается связано значительными силами с двумя атомами, образуя водородную связь между ними. Энергия такой связи приблизительно равна 0,1 эВ [74].
В общем случае электроотрицательный атом (т. е. атом, способный притягивать электроны), оттягивая электрон связи от ядра атома водорода, приобретает отрицательный заряд. Водород при этом приобретает положительный заряд, равный заряду протона. Этот протон и осуществляет связь между атомами (рис. 2.11). Малые размеры ядра атома водорода не позволяют ему иметь ближайшими соседями более чем два атома. Поэтому водородная связь осуществляется только между двумя атомами. Типичным примером может служить водородная связь, возникающая между молекулами воды (рис. 2.12).
|
|
|
|
Рис. 2.11. Водородная связь в молекуле HF2 |
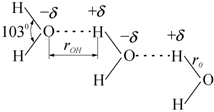
Рис. 2.12 Водородная связь между молекулами воды [74] |
Связь
O−H, устанавливающаяся между атомом кислорода одной молекулы воды и
атомом водорода другой молекулы, ведет себя как маленький диполь с зарядом –d на кислороде и +d на водороде. Притяжение между этими зарядами и приводит к
возникновению водородной связи, показанной на рис. 2.12 точками. Водородная
связь имеет направленный тетраэдрический характер. Притяжению способствуют
малые размеры атома водорода, позволяющие ему сблизится с электроотрицательным
атомом. Тем не менее данное расстояние ![]() значительно больше
длины
значительно больше
длины ![]() ковалентной связи
H−O в самой молекуле воды, равной 0,96 Å. Это объясняется тем, что
энергия ковалентной связи примерно на порядок выше энергии водородной связи.
ковалентной связи
H−O в самой молекуле воды, равной 0,96 Å. Это объясняется тем, что
энергия ковалентной связи примерно на порядок выше энергии водородной связи.
Водородная связь вызывает ассоциацию молекул жидкостей (воды, кислот, спиртов и др.), приводящую к повышению их вязкости, увеличению точки кипения, аномальному изменению объема при нагревании.