2.3.4. Ван-дер-Ваальсова связь. Молекулярные кристаллы
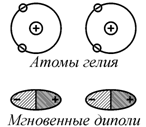
К веществам с молекулярной связью относятся кристаллы, в узлах кристаллической решетки которых располагаются либо одинаковые молекулы с насыщенными связями (H2, Cl2, Br2, I2), либо атомы инертных газов (Ar, Ne, Xe, Rn). Характерная особенность молекулярных кристаллов состоит в том, что частицы в кристалле удерживаются очень слабыми силами Ван-дер-Ваальса. В атомах инертных газов электроны образуют очень прочные устойчивые группировки из восьми электронов в состоянии s2p6, поэтому на их движение присутствие соседних атомов влияет слабо. В среднем распределение заряда имеет сферическую симметрию, когда атомы находятся достаточно далеко друг от друга. При сближении атомов симметрия нарушается, и возникает мгновенный дипольный электрический момент (рис. 2.10), который создает в центре другого атома электрическое поле, которое также приводит к возникновению в нем дипольного момента [74].
Таким образом, при сближении атомов стабильная конфигурация представляет собой два электрических диполя. Результатом является притяжение между атомами. Лондоном был выполнен квантовомеханический расчет энергии взаимодействия. Им было установлено, что полная энергия двух взаимодействующих осцилляторов уменьшается по причине взаимодействия на величину, обратно пропорциональную шестой степени расстояния между ними.
|
|
Рис. 2.10. Образование молекулы гелия при сближении двух атомов |
При
дальнейшем уменьшении расстояния между атомами их электронные оболочки начинают
перекрываться, и они испытывают отталкивание. В случае инертных газов оно появляется
в основном в результате действия принципа Паули: два электрона не могут иметь
одинаковые квантовые числа, т. е. не могут занимать одну и ту же область
пространства без увеличения их кинетической энергии. Это приводит к возрастанию
полной энергии системы и к появлению сил отталкивания. Полную потенциальную
энергию взаимодействия двух атомов принято записывать в виде (2.10), где а и b − положительные
постоянные, а показатели степени зависят от вида взаимодействия атомов.
Напомним, что ![]() − потенциал притяжения,
− потенциал притяжения, ![]() − потенциал отталкивания.
− потенциал отталкивания.
Полную потенциальную энергию в случае вандерваальсова кристалла можно
записать в виде:
|
|
(2.28) |
Обычно для описания взаимодействия нейтральных атомов и неполярных молекул используют потенциал Леннарда−Джонса
|
|
(2.29) |
где 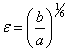 , а
, а ![]() − соответствует
межатомному расстоянию, при котором полная потенциальная энергия равна нулю.
Параметр e
имеет размерность энергии и равен минимуму потенциальной энергии при
− соответствует
межатомному расстоянию, при котором полная потенциальная энергия равна нулю.
Параметр e
имеет размерность энергии и равен минимуму потенциальной энергии при ![]() . Коэффициент s можно рассматривать и как радиус сферы
непроницаемости взаимодействующих атомов, а
. Коэффициент s можно рассматривать и как радиус сферы
непроницаемости взаимодействующих атомов, а ![]() как радиус действия
межатомных сил. Величины s
и e
получают из эксперимента или рассчитывают аналитически (табл. 2.5 [78]).
как радиус действия
межатомных сил. Величины s
и e
получают из эксперимента или рассчитывают аналитически (табл. 2.5 [78]).
Таблица 2.5
Теоретические и
экспериментальные значения параметров
Леннарда-Джонса и энергий сцепления молекулярных кристаллов
|
Кристалл |
|
e, эВ |
r0×10-1, нм |
U0, эВ |
||
|
эксперимент. |
теоретич. |
эксперимен. |
теоретич. |
|||
|
Ne |
2,74 |
0,0031 |
3,14 |
2,99 |
-0,020 |
-0,027 |
|
Ar |
3,40 |
0,0104 |
3,75 |
3,71 |
-0,08 |
-0,089 |
|
Xe |
3,98 |
0,0200 |
4,35 |
4,34 |
-0,17 |
-0,172 |
Наибольшие расхождения экспериментальных и теоретических значений,
приведенных в табл. 2.5, связаны с тем, что при аналитическом расчете не учтены
нулевые колебания атомов при ![]() . Видно, что, чем выше масса атома, тем больше энергия
сцепления, а, следовательно, и температура плавления молекулярного кристалла.
Например, при комнатной температуре фтор (порядковый номер атома в таблице
Менделеева
. Видно, что, чем выше масса атома, тем больше энергия
сцепления, а, следовательно, и температура плавления молекулярного кристалла.
Например, при комнатной температуре фтор (порядковый номер атома в таблице
Менделеева ![]() ) – газ, бром (
) – газ, бром (![]() ) – жидкость, а йод (
) – жидкость, а йод (![]() ) – кристалл.
) – кристалл.
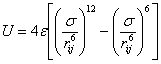 ,
,