1.5. Принцип плотной упаковки атомов
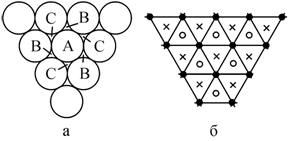
Атомы и ионы большинства химических элементов обладают сферической симметрией. Если атомы представить в виде малых твердых несжимаемых шаров, между которыми действуют силы взаимного притяжения и отталкивания, то особенности строения большинства кристаллов можно условно рассматривать как пространственную упаковку таких шаров. Шары укладываются так, чтобы упаковка обладала наибольшей симметрией и компактностью. Это условие выполняется, если каждый шар соприкасается с шестью шарами. При этом в плоском слое каждый шар окружен шестью треугольными лунками (пустотами), а каждая из лунок − тремя шарами (рис. 1.15) [54, 74]. Обозначим шары буквами А, а пустоты − буквами В и С.
|
|
|
Рис. 1.15.
Плотная упаковка шаров: а −
плоский слой шаров одинакового радиуса; б − тот же слой, представленный
в виде сетки, узлами которой являются центры треугольных пустот, |
Каждая из пустот типа В и С окружена
тремя шарами, следовательно, каждому из этих трех шаров она принадлежит на одну
треть. Значит, на каждый шар приходится ![]() пустоты. Если
укладывать следующий слой шаров, то их можно располагать так, чтобы каждый шар
следующего слоя лег бы в лунку, образованную тремя соседними шарами. Поскольку
треугольных пустот в два раза больше, чем шаров, то следующий слой можно
расположить двумя способами: либо в углублениях В, либо С. Такая ситуация
возникает при укладке каждого следующего слоя, следовательно, существует
бесконечное число возможностей упаковывать шары, причем каждой из них должна
соответствовать одна и та же плотность заполнения пространства шарами, равная
74,05 %.
пустоты. Если
укладывать следующий слой шаров, то их можно располагать так, чтобы каждый шар
следующего слоя лег бы в лунку, образованную тремя соседними шарами. Поскольку
треугольных пустот в два раза больше, чем шаров, то следующий слой можно
расположить двумя способами: либо в углублениях В, либо С. Такая ситуация
возникает при укладке каждого следующего слоя, следовательно, существует
бесконечное число возможностей упаковывать шары, причем каждой из них должна
соответствовать одна и та же плотность заполнения пространства шарами, равная
74,05 %.
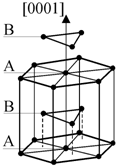
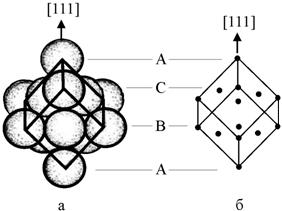
Однако среди большого числа реальных кристаллических структур число таких упаковок ограничено. Чаще всего встречаются плотнейшая гексагональная (рис. 1.16) и плотнейшая кубическая (рис. 1.17) упаковки. В гексагональной плотноупакованной (ГПУ) структуре слой В повернут на 60о относительно слоя А. Последовательность укладки в этой структуре АВАВАВ… или АСАСАС... В кубической упаковке слои располагаются перпендикулярно направлению [111] в гранецентрированной кубической (ГЦК) решетке и чередование слоев имеет вид АВСАВСАВС...
|
|
|
|
Рис. 1.16.
Гексагональная |
Рис. 1.17.
Кубическая плотная упаковка: а −
упаковка шаров в ГЦК структуре; |
Для использования принципа плотной упаковки в качестве модели структуры кристаллов необходимо учитывать число и вид пустот, окружающих каждый атом. В плоском слое на шар приходится две треугольные пустоты, в пространстве каждый шар окружают пустоты двух сортов: тетраэдрические и октаэдрические.
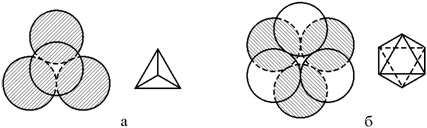
Если треугольную пустоту плоского слоя прикрыть сверху третьим шаром, то пустота в обоих слоях оказывается окружена четырьмя шарами, центры которых образуют правильный тетраэдр. Такая пустота называется тетраэдрической (рис. 1.18, а). Если же треугольная пустота второго слоя шаров находится над пустотой первого слоя, тогда возникающая при этом пустота окружена шестью шарами, располагающимися по вершинам октаэдра. Соответственно пустоту называют октаэдрической (рис. 1.18, б).
Число тетраэдрических пустот в
плотнейшей упаковке в два раза больше числа октаэдрических. Докажем это
утверждение. Каждая октаэдрическая пустота окружена в пространстве шестью
атомами, а каждый атом окружен шестью октаэдрическими пустотами. Таким образом,
каждая такая пустота принадлежит данному атому на ![]() и, следовательно, на
каждый атом приходится
и, следовательно, на
каждый атом приходится ![]() октаэдрическая
пустота. С другой стороны, каждый атом одновременно окружен восемью
тетраэдрическими пустотами, а каждая из них окружена четырьмя атомами.
Следовательно, на каждый атом приходится
октаэдрическая
пустота. С другой стороны, каждый атом одновременно окружен восемью
тетраэдрическими пустотами, а каждая из них окружена четырьмя атомами.
Следовательно, на каждый атом приходится ![]() тетраэдрические
пустоты.
тетраэдрические
пустоты.
|
|
|
Рис. 1.18.
Пустоты в плотной упаковке шаров: а –
тетраэдрическая; б – октаэдрическая пустоты (шары нижнего слоя заштрихованы)
[74] |
Доля пространства, занимаемого
атомами элементарной ячейки от объема ячейки называется коэффициентом упаковки ![]() [%], где
[%], где ![]() - объем,
занимаемый атомом,
- объем,
занимаемый атомом, ![]() - количество атомов, приходящихся на
элементарную ячейку,
- количество атомов, приходящихся на
элементарную ячейку, ![]() -
объем элементарной ячейки.
-
объем элементарной ячейки.
Важной характеристикой
кристаллической структуры является координационное
число n, которое равно числу ближайших соседей, окружающих данный атом.
Например, в кубической и гексагональной плотных упаковках ![]() , а коэффициент упаковки
, а коэффициент упаковки
![]() %. В кубической
объемноцентрированной структуре
%. В кубической
объемноцентрированной структуре ![]() ,
, ![]() %.
%.
В модели плотноупакованной структуры существует возможность размещения между основными атомами атомов меньшего размера так, чтобы они касались окружающих атомов. Если принять радиус основного шара за единицу, то радиусы шаров, которые можно разместить в тетраэдрических и октаэдрических пустотах составляют соответственно 0,22 и 0,41.
Принцип плотной упаковки атомов играет важную роль в определении типа кристаллических структур различных классов веществ. Этот принцип определяет конфигурацию частиц в тех случаях, когда между ними действуют ненасыщенные и ненаправленные связи. В этих случаях энергетически более выгодны структуры с возможно большими координационными числами. С точки зрения плотнейшей упаковки, например, особенно просто описываются структуры окислов сульфидов и галогенидов, основу плотнейшей упаковки в которых составляют крупные анионы кислорода, серы и галогенов. Катионы, входящие в кристалл, распределяются в пустотах плотнейшей упаковки по определенному симметричному узору.
1Для описания гексагональных кристаллов принято пользоваться
четырехосной системой координат, вводя дополнительную ось u, которая составляет равные углы (120о)
с осями x и y и параллельна оси z. Символы
направлений в этом случае задаются четырьмя индексами [mnip].